最新《Science》!体内超声3D打印
导读:3D打印为患者量身定制植入物和治疗方案带来了新希望,但传统方法往往依赖侵入性手术,限制了其广泛应用。为克服这一难题,一种成像引导的深层组织体内声音打印平台(DISP)应运而生。

2025年5月9日,据资源库了解,来自加州理工学院的研究人员成功开发出一种新型体内3D打印技术—— DISP(深层组织体内声学打印平台),据称该方法不仅可用于药物和细胞递送的生物粘附凝胶及聚合物外,还被用于打印生物电水凝胶。这一研究成果近日发表于《科学》(Science)期刊。

链接:www.science.org/doi/10.1126/science.adt0293
此前的体内3D打印研究多依赖红外光触发聚合反应,激活聚合物单体形成固态结构。但由于红外线穿透能力有限,仅适用于皮下层级。DISP平台则通过将载有交联剂的低温敏感脂质体集成至生物墨水中,利用聚焦超声实现多种功能性生物材料的高精度、快速且可按需交联。
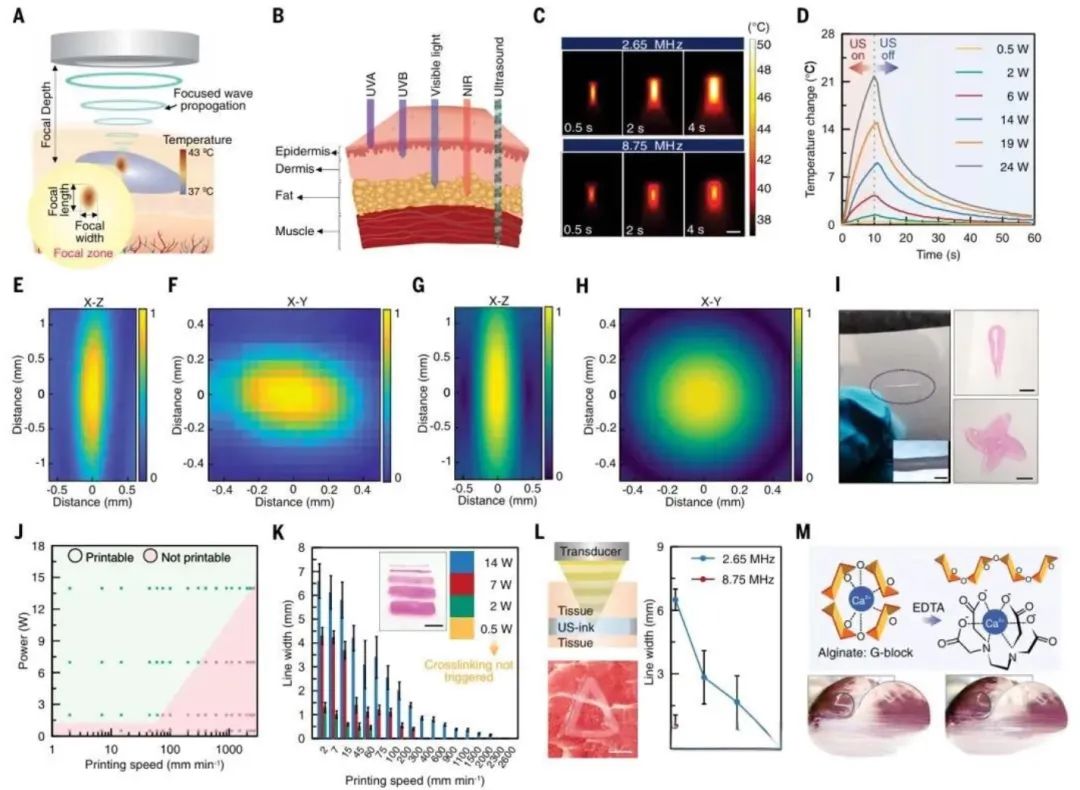
同时,DISP结合了基于气囊的超声成像技术,能够提供实时监控,并支持在活体动物体内打印出定制化结构。
一项全新理念的诞生
DISP平台的核心创新在于其对聚合反应的空间与时间可控性。团队通过引入聚焦超声波与低温敏感脂质体的结合,实现对材料聚合位置的精确控制。脂质体是一种常见药物递送载体,在本研究中被用作交联剂的微型容器,随后被掺入生物墨水中。该墨水同时含有聚合物单体、显影造影剂以及待递送的活性物质,如药物、细胞或导电材料(如碳纳米管、银颗粒等)。

注射入体后,通过将目标区域温度提升约5°C,超声波触发脂质体释放交联剂,进而启动局部聚合过程,实现“原位成形”的体内打印。
为实现对体内聚合反应的可视化监测,团队还引入了源自细菌的蛋白质“气囊”作为超声造影剂。这些充气囊泡不仅在影像中清晰可见,还能感知材料从液态到凝胶状态的变化。通过对成像对比度的分析,研究人员能够实时判断聚合是否完成、打印是否成功,极大提升了体内操作的精度与安全性。
药物递送与未来的临床前景
在验证实验中,研究团队在小鼠膀胱肿瘤周围区域利用DISP平台打印了载有阿霉素的药物水凝胶。结果显示,相较于传统药物注射,该方式能显著提高局部肿瘤细胞的凋亡率。
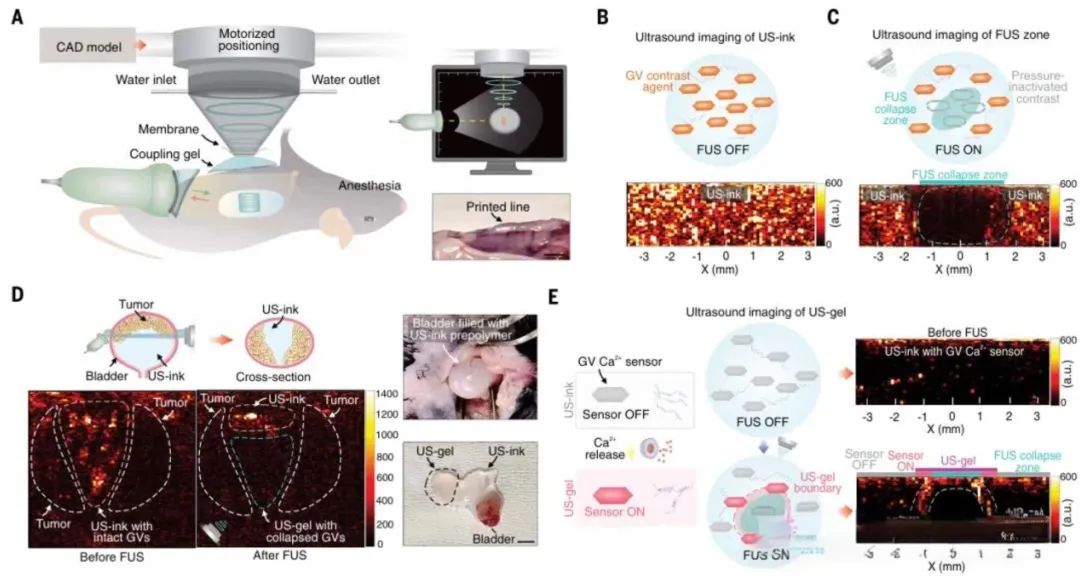
“我们已经在小动物模型中证明DISP用于肿瘤治疗的有效性,”加州理工学院医学工程系教授高伟指出,“下一步将扩展至大动物模型,最终推动临床转化。”此外,团队也在探索将人工智能与DISP平台融合,提升其在动态器官(如心脏)中的自动定位与实时打印能力。“未来,我们希望借助机器学习,实现真正意义上的自主化体内打印。”他说。

事实上,关于声音3D打印的研究早已有所探索。例如,早在2022年6月,康考迪亚大学的研究团队便提出了“直接声音打印(Direct Sound Printing, DSP)”技术,通过超声波实现对液态树脂的空间定位与固化,首次展现出利用声波制造复杂结构的潜力,该成果发表在《自然通讯》。随后在2024年10月,该校研究人员进一步提出“全息直接声音打印(Holographic DSP, HDSP)”,通过构建三维声场实现更高精度的非接触式打印,同样发表于《自然通讯》。
而此次加州理工学院开发的DISP平台,不仅继承了超声驱动打印的技术路径,更进一步将其推向活体环境下的深层组织打印,具备了真正的临床前应用可能。
 云霞育儿网
云霞育儿网
发表评论:
◎欢迎参与讨论,请在这里发表您的看法、交流您的观点。