本文为《大美界》原创
作者|秦思樾
最近,“萝莉岛”事件再度进入公众视野,其中涉及富豪通过注射干细胞、甚至尝试器官替换以追求青春永驻的传闻。
这类故事并非孤例——从硅谷大佬换血延寿,到黑市胎盘交易、尸体材料盗卖,人类对于“抗衰老”与“再生”的痴迷,早已演变成一场混杂着前沿科技、伦理灰色地带与资本狂热的复杂图景。
在这场看似荒诞的“续命竞赛”背后,一项名为“诱导性多能干细胞(iPSC)”的技术,正悄然从实验室走向临床,甚至被一些人奉为“器官自由”乃至“肉体重塑”的钥匙。
据Grand View Research全球iPSC治疗市场规模2022年15亿美元,CAGR为10.61%,2030年预计高达到31亿美元。
它究竟是未来医学的曙光,还是又一个被过度包装的科学幻想?
1
iPSC是什么?
先要回答一个问题。人为什么会衰老?
细胞是人体组成的最小单位,人体衰老的根源就在细胞。
在人体内每分钟大约有1亿个细胞死亡,死亡的细胞需要得到及时补充,人体生长伤口愈合等生理病理活动也需要新细胞。
那么问题来了,新细胞从哪里来?
最重要的源泉就是各种干细胞,干细胞也因此被称作“生命的种子”。
2006年以前,想要获得干细胞,要么从正常发育的胚胎中提取,要么借助于体细胞核移植重编程技术——也就是所谓的“克隆”,但这两种方法都会扼杀一个具有出生潜力的胚胎。
伦理问题的软肋成为干细胞研究和应用无法逾越的鸿沟。
2006年,日本科学家山中伸弥发明的诱导性多能干细胞技术(iPSC ),将“成年”版本的细胞逆向诱导为具有更多可能性的“婴儿期”版本细胞,巧妙地绕开了一切伦理问题。他也因此斩获了2012年诺贝尔生理学或医学奖。
2008年《本杰明·巴顿奇事》上映,电影中描绘的婴儿从古稀老人状态越长越年轻,到最终变成婴儿死去,与iPSC的发明和应用形成一种时空呼应——“人的细胞可以越活越年轻”。
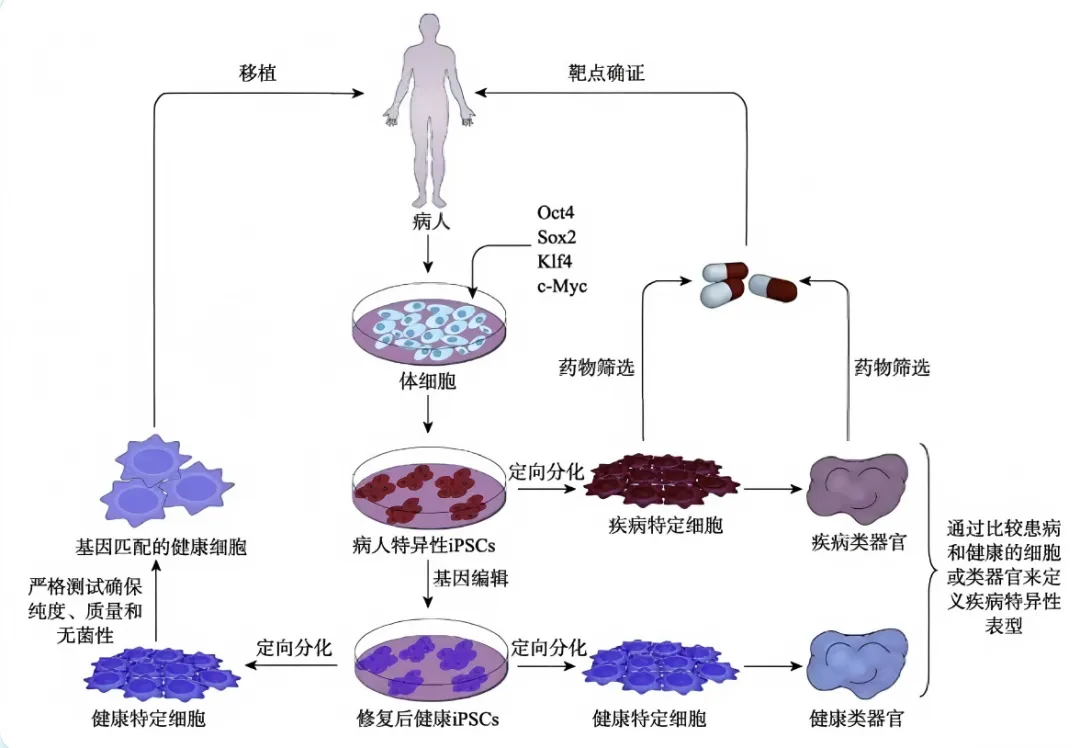
这项技术通过人工诱导的方法将四个精心筛选得来的因子导入到体细胞中,进行重编程逆分化培养出的一类具有类胚胎干细胞特征的多能干细胞,可以分化成多种功能细胞,并在体外培养获得心肌细胞、神经元细胞、胰岛细胞等表型细胞。

iPSC分化路径; 图源:360doc.com
相较于胚胎干细胞,iPSC的优势极为显著:可以在体外无限复制,适用于大规模培养;iPSC可根据需求诱导分化成需要的细胞株,批次间特性相对稳定,可避免临床疗效不一致情况的发生;iPSC来源于患者自身,可减小免疫排斥问题;iPSC来源于成体细胞,还避免了伦理问题。
星星之火,可以燎原。
在山中伸弥之后,全世界也掀起了iPSC的狂潮,到现在已经有4000多篇文章发表,后续的研究还在井喷式的发展。
这背后还得益于iPSC的技术优势——成熟简单且相对便宜,传统的核移植除了要求要非常熟练的经验和完备的实验室、优质的实验动物,而iPSC把技术门槛降低了很多,让很多普通实验室也能尝试成功。
2
如何得到“返老还童”的细胞?
这里先理解重编程。
每一个细胞的细胞核都包含有这个生物个体的几乎所有的遗传信息(有部分存在于线粒体中),这些遗传信息决定了我们可以发育成什么样的个体,这就是“细胞核的全能性”。
对每个细胞来说,它们的DNA序列虽然都是一样的,但是它们的DNA、染色体及核蛋白的模式、结构和修饰(化学修饰,比如甲基化、乙酰化、磷酸化和糖基化等)却不一样,而这些差异导致了细胞的命运不一样:有的能分化成多种细胞,有的就只能行使一种功能。
在高等生物发育的过程中,DNA、染色体以及核蛋白的改变基本上是一个不可逆的程序化的过程。想要得到“返老还童”的细胞,所以有了“重编程”这个概念。
iPSC提取方法; 图源:医药魔方
目前,用于重编程的体细胞主要来源于血液、皮肤、尿液,各有优劣。血液被认为是应用较多且相对简单的细胞来源;皮肤的优势在于获取简单,但皮肤会受到紫外线照射等因素影响,细胞突变较多;尿液便利无创,但细胞含量相对较少且质量不如血液中的新鲜细胞。
另外,因个体基因差异的存在,不同细胞适用于不同方向,像瘦人体细胞做成的胰岛可能比胖人体细胞做成胰岛效果要更好。
iPSC重编程方法众多,根据是否将转录因子整合到细胞基因中,可分为整合重编程技术(慢病毒、逆转录病毒等)和非整合重编程技术(游离型载体、仙台病毒、mRNA、miRNA、蛋白质、其他小分子等)。因使用的技术路线不同,在重编程效率、材料制备、递送过程及安全性等方面各具特点。
以小分子重编程为例,它的优势在于稳定性和安全性较好,从生产工艺上来讲相对简单,且成药性也更好,其劣势也很明显:如果涉及多个成分,检测成本也会相应增加。

iPSC技术路径; 图源:沙利文报告
iPSC携带了人类全套基因,在相关诱导技术和培养条件成熟后,可根据需求分化为相应的细胞、类器官、器官,甚至是完整的生命个体,形成“克隆人”。
我们可以畅想,未来,所有人体器官都可以生产制造,器官衰竭将不再是生命终点,更换器官会是司空见惯,就像给车更换零件一样,而且不用他求,就用自己的细胞治疗自己的疾病,只要自己愿意。
理想已然照进现实,科学家们已经基于iPSC技术首创性地解决了很多的临床难题,多款基于iPSC技术的细胞治疗产品进入临床试验阶段。
研究人员也表示,形成完整的三维器官很复杂,涉及到不同的细胞类型以及对应的配比,还须进行3D打印,但克服这些难点也只是时间问题。
如果这项技术广泛应用尚有距离,那当下的我们还能做点什么呢?
现在可以存储iPSC,为未来买一份健康保险。年轻时存储并制备健康的细胞,可保留最佳的细胞状态,为未来治疗提供有力保障,万一哪天你需要用器官,年轻时候的细胞培养出来的往往更好。
相比于脐血干细胞的获取渠道有限、只能分化成造血干用于特定用途,也只能供一定体重范围内的用量,iPSC可以从身体上轻易获取,还能诱导成大部分专能干细胞,且随时取用传代4-5代几乎不限量,应用价值更为广泛。
目前存储iPSC市场价已经达到100万人民币,涉及环节包括细胞采集与制备、质量控制与鉴定、扩增培养、冷冻保存与长期存储、存储后的应用潜力评估;已经形成了完整的产业链,包括技术与原料供应商、iPSC制备/存储与开发服务商、应用终端等。
其实,从普通人的角度,大部分人或多或少都有遗传缺陷,iPS细胞的“重编程”未来也有望多方位的“改造”自身缺陷。
目前,凭借其独特的优势,iPSC来源的细胞疗法已成一个主流发展方向之一。据Clinicaltrials.gov数据显示,中国已有近40家企业布局iPSC领域。
虽然目前美国在一些技术应用上可能更快,而中国在一些细分领域,譬如修复血管等方面有自己的独特优势,并形成了一股投资热潮。
3
准备好迎接革命式抗衰了吗?
不过,任何技术都不是万能的。iPSC在保证安全、优化效率等方面仍存在瓶颈。
首先,分化效率。
iPSC从当下的转录组学和表观组学状态转变到目标细胞的状态,相关条件还很苛刻,具有较高的技术壁垒;
其次,成瘤性。
iPSC虽然能分化成不同类型的体细胞,但若移植后过度增殖可能导致肿瘤形成。2022年,《Stem Cells and Development》杂志就曾刊登一篇病例报告,云南省肿瘤医院接诊了一例在其他医疗机构接受iPSC衍生细胞治疗后出现不成熟畸胎瘤的患者。
接着,免疫原性。
目前受制备成本和临床急迫性的限制,iPSC的应用项目中多使用异体细胞,免疫原性问题不可忽视。
据了解,人群中存在一类“超级供体”,其HLA(人类白细胞抗原)基因5位点是高频单倍体纯合子,基于这些供体制备的细胞可覆盖高数量的受体人群。
目前,多个国家及地区已建立了iPSC超级供体库,我国也在2018年制备完成首例由“超级供体” 诱导的多能干细胞株,制备适用于所有受体人群的通用细胞系。
最后,异质性。
iPSC在培养后不同细胞系之间的形态、生长曲线、基因表达和分化等方面会有差异,出现异质性,阻碍相关药物的批量生产。
另外,这些新技术应用要走正规途径、避免滥用。
当然,任何伟大的技术在爆发前夜,都难免伴随着泡沫与杂音。目前的iPSC市场,确实存在着虚假宣传与过度包装的乱象。但这并不应成为我们否定未来的理由。
未来3-5年将是iPSC临床成果的井喷期,而6-10年后,或许我们将真正迎来“器官工厂”的落地。
在这场与时间的赛跑中,科学家负责突破上帝的禁区,监管者负责守住安全的底线,而资本则负责为这场漫长的远征提供粮草。
对于我们每一个人而言,关注iPSC,不仅仅是关注一种疗法,更是在见证人类如何一步步将“革命式抗衰”照进现实。

——END——