PART1
临床痛点:不同方法学检测结果不一致

子宫内膜癌(EC)分子分型已成为NCCN、ESGO-ESTRO-ESP指南推荐的常规诊断项目,其中错配修复缺陷(dMMR)/微卫星高度不稳定(MSI-H)亚型因对免疫治疗敏感,其精准识别直接影响治疗策略制定。临床常用免疫组化(MMR-IHC)检测MLH1、MSH2、MSH6、PMS2蛋白表达,或通过NGS/PCR检测MSI状态,但两者结果不一致的情况屡见不鲜。
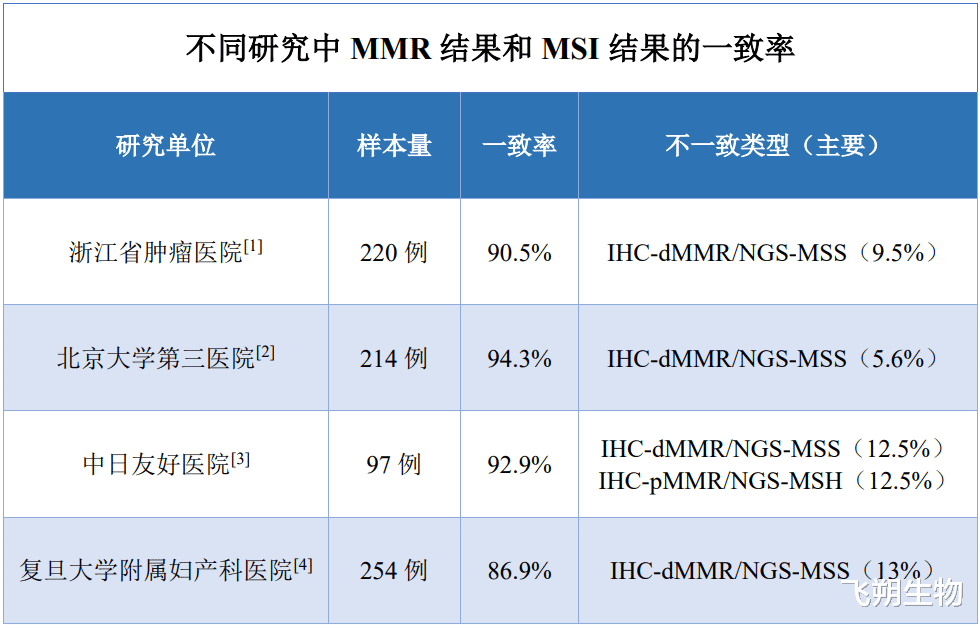
值得注意的是,所有不一致病例中,IHC提示dMMR但MSI检测为MSS(微卫星稳定)占绝对主导(90%以上),反向不一致(IHC-pMMR/MSI-H)罕见,这一特征为机制解析提供了重要线索。
PART2
技术原理差异
01.检测靶点与维度的本质区别
MMR-IHC:评估蛋白表达层面,通过抗体识别MMR蛋白是否存在,间接推断修复功能。优势是操作简便、成本低,但无法区分“蛋白缺失”与“功能缺陷”的因果关系。
MSI检测(NGS/PCR):评估DNA功能层面,通过检测微卫星重复序列的插入/缺失,直接反映错配修复系统的实际功能状态。但受检测位点选择、测序深度、算法阈值影响较大。
02.方法学局限性导致的假结果
IHC假阳性风险:部分MMR蛋白存在“免疫反应性但功能失活”的变异体,如MSH6的某些错义突变可能保留抗原性但丧失修复功能,导致IHC误判为pMMR(罕见);或因组织固定不当、抗原修复不足导致蛋白表达误判为缺失。
MSI假阴性风险:NGS面板设计若未覆盖高灵敏度微卫星位点,或测序深度<500×,可能漏检低水平MSI;PCR检测对样本DNA质量要求高,降解样本易导致结果偏差。
PART3
不一致原因解析
一般而言,dMMR对应MSI-H表型,pMMR表现为MSI-L或MSS。文献报道恶性肿瘤中MMR与MSI检测符合率因瘤种不同而有差异,
在子宫内膜癌中检测结果的不一致性较为突出,约占10%。MMR免疫组化与MSI分子检测结果不一致可分为两类,一类是pMMR出现MSI-H,另一类是dMMR出现MSI-L或MSS,并未出现MSI-H,前者更常见。常见不一致发生的原因总结如下。
01.肿瘤异质性与亚克隆缺失
12%的不一致病例源于MMR蛋白亚克隆缺失(如肿瘤局部区域蛋白缺失,整体样本MSI检测为MSS),这与肿瘤演进过程中的克隆选择有关;中日友好医院研究[3]发现,8.2%的病例存在多重分子分型(如POLE mut+MSI-H),亚克隆层面的MMR缺陷可能被其他驱动突变(如POLE)掩盖,导致检测结果矛盾。
02.POLE共突变的干扰
当POLE基因的核酸外切酶结构域发生致病性突变时,POLE蛋白在DNA复制过程中无法及时执行错配校正功能,导致肿瘤细胞基因组DNA出现大量复制错误。少数EC病例发现因POLE外切酶结构域突变造成患者出现MSI-H而MMR蛋白仍保留的情况,考虑可能是POLE外切酶结构域突变导致了MMR基因突变,继而出现MMR蛋白功能缺陷,从而导致MSI-H,但MMR蛋白的功能缺陷并未被常规免疫组化检测识别出来。
03.MMR蛋白功能异常但抗原活性保留
有研究表明一些MMR蛋白由于基因发生剪接位点和移码突变导致功能异常,从机制上来讲,其可能编码了结构和功能均有缺陷的蛋白,但是抗原活性仍能被相应的抗体免疫组化检测识别,4种MMR蛋白均显示阳性,MSI检测为MSI-H[5]。
04.MMR蛋白缺失其功能被代偿
MSH2与MSH6或MSH3分别形成MutSα或MutSβ异源二聚体,两者均为在错配识别和修复启动中起关键作用的ATP酶;MLH1与PMS2、PMS1或MLH3分别形成其他异源二聚体,具有切除DNA复制过程中错配的碱基的作用。其中,MSH6的功能可以被MSH3代偿,在浙江肿瘤医院研究发现,43.8%(7/16)的不一致病例表现为孤立MSH6缺失,其MSI检测为MSS或MSI-L[1]。当MSH6和PMS2蛋白因其基因突变造成功能缺陷时,其他复合物则可以对错配的基因进行修复。所以,免疫组化检测到MSH6和(或)PMS2蛋白表达缺失有时并不影响微卫星状态的稳定[5]。
05.MLH1启动子甲基化
北大三院研究显示,66.7%(6/9)的不一致病例存在MLH1启动子高甲基化,导致MLH1/PMS2蛋白共缺失,但MSI检测为MSS:散发性dMMR子宫内膜癌中,70%-80%的MLH1缺失由启动子甲基化引起,而非基因突变;甲基化导致的MLH1表达沉默可能是不完全的,或仅发生在肿瘤亚克隆中,不足以引发广泛的微卫星不稳定;此类病例需与林奇综合征鉴别:林奇综合征相关MLH1缺失多由胚系突变引起,无启动子甲基化,且TMB显著更高(71.5±20.1 vs 41.9±24.3mut/Mb,P=0.001)[2]。
06.MMR蛋白免疫组化检测问题
目前病理科只检测MLH1、MSH2、MSH6和PMS2这4种核心蛋白是否表达。除这4种蛋白之外的MMR蛋白缺失及功能缺陷也可能会导致MSI-H。肿瘤细胞含量<30%的样本,IHC易受间质细胞干扰,甲醛固定时间过长(>48h)会导致DNA交联、蛋白抗原性丢失,显著增加不一致风险(发生率升高3.2倍)。还有抗体选择,人工判断都会导致结果存在差异。
07.MSI检测问题
PCR检测MSI单核苷酸位点不足导致敏感度不够,MSI检测易因正常细胞DNA稀释导致假阴性,与结直肠癌相比,EC的MSI-H状态更多地由最小微卫星位移导致。这种由1-3个核苷酸变化引起的细微变化,容易导致错误地将EC中MSI-H判读为MSI-L或MSS。
08.检测时机与治疗干扰
新辅助化疗后,肿瘤组织发生坏死、纤维化,可能导致MMR蛋白表达异常或MSI信号改变,建议检测优先使用治疗前活检样本;激素治疗可能上调MSH3表达,增强对MSH6缺失的补偿作用,导致MSI检测结果逆转。
PART4
总结
MMR与MSI均是预测肿瘤免疫治疗反应、筛选Lynch综合征及对子宫内膜癌进行分子分型的不可或缺的指标。然而MMR-IHC与MSI检测本质分别是“蛋白表达”与“功能状态”,其检测原理与内在机制的微妙差异,导致在特定子宫内膜癌病例中展现出不一致的检测结果。因此在临床实践中更需要多种方法学进行检测,进行结果相互验证,避免单一检测导致的分型误判。
参考文献
[1] Xi Y, He C, Fang X, Yin JC,
Wang Y, Wang H, Wu C, Fang J, Lai Q, Liu P, Chu F, Yin W, Su D. Analysis of
discordance between mismatch repair and microsatellite instability testing in
endometrial cancer. Hum Pathol. 2026 Feb;168:106004. doi: 10.1016/j.humpath.2025.106004.
Epub 2025 Dec 8. PMID: 41371509.
[2]刘岩,王玉湘,孙小婕,等.子宫内膜癌分子分型中错配修复和微卫星不稳定性状态的综合评估.中华妇产科杂志,2023,58(10):755-765.
DOI:10.3760/cma.j.cn112141-20230711-00316
[3]王晓伟,林洁,陈皇,等.子宫内膜癌分子分型的临床病理及遗传分子表型特征分析.中华肿瘤杂志,2025,47(01):100-107.
DOI:10.3760/cma.j.cn112152-20231024-00225
[4]陈婷婷,陶祥,刘天齐,等.二代测序和免疫组织化学在子宫内膜癌分子分型中的比较.中华病理学杂志,2023,52(06):580-585.
DOI:10.3760/cma.j.cn112151-20230303-00166
[5]王 宇,白艳花.子宫内膜癌错配修复蛋白与微卫星状态检测结果不一致性原 因分析[J].临床与实验病理学杂志,2024,40(09):913-916.DOI:10.13315/j.cnki.cjcep.2024.09.004
声明:本文仅用于分享,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!