双特异性抗体(Bispecific antibodies, bsAbs)作为新一代工程化抗体的核心代表,打破了传统单克隆抗体(mAbs)“单一抗原结合” 的局限,通过基因工程技术在单个抗体分子中构建两个不同的抗原结合位点,实现对两种不同抗原表位的同时靶向。这种独特设计赋予其 “桥接” 功能,既能精准聚焦病变靶点、增强治疗特异性,又能克服传统化疗与单抗疗法面临的耐药性、非特异性毒性等痛点,在肿瘤治疗、自身免疫病干预、临床诊断及医学影像等领域展现出全方位的应用潜力,成为生物医学领域的研发热点与转化核心。
一、核心作用机理:两类双抗的靶向逻辑与功能差异双特异性抗体的功能实现依赖其精准的作用机理设计,根据核心作用模式可分为两大类别,分别适配不同的疾病干预需求:一类是抗原交联型(antigen crosslinking)双抗,其两个结合位点靶向两种不同的抗原,通过信号阻断、受体调控或免疫逃逸抑制发挥作用。在肿瘤治疗中,这类双抗可同时靶向肿瘤细胞表面的关键驱动靶点,如 amivantamab 同时结合 EGFR 与 c-MET,通过阻断两条异常激活的信号通路、诱导受体降解,双重抑制肿瘤增殖;也可靶向免疫检查点分子,如 PD-1/CTLA-4 双抗,同时解除 T 细胞的双重免疫抑制,激活机体自身的抗肿瘤免疫应答。在传染性疾病领域,中和型双抗通过靶向病毒表面的不同关键抗原(如 HIV 的 gp120 与 gp41),形成 “双重封锁”,有效防止病毒通过抗原变异实现免疫逃逸,提升抗病毒效果。这类机制无需直接招募免疫细胞,核心优势在于增强靶向特异性与作用强度。
另一类是细胞桥接(Cell-Bridging)型双抗,核心功能是搭建免疫细胞与靶细胞的 “沟通桥梁”,以 T 细胞衔接器(T cell engager, TCE)为代表,还衍生出 NK 细胞衔接器(NKCE)、巨噬细胞衔接器(MCE)等多种类型。其设计逻辑是 “一端靶向肿瘤相关抗原(Tumor-associated antigen, TAA),一端靶向免疫细胞表面的激活分子”:例如靶向 T 细胞表面 CD3 或 NK 细胞表面 CD16 的双抗,可将免疫细胞直接招募至肿瘤细胞附近,形成 “免疫突触”,激活免疫细胞释放穿孔素、颗粒酶等杀伤分子,实现对靶细胞的特异性清除。经典药物 blinatumomab 便是这一机制的典型代表,通过桥接 CD3+ T 细胞与 CD19+ B 细胞,高效诱导 T 细胞介导的细胞毒性,在血液肿瘤治疗中展现出显著疗效。
二、多领域应用:从治疗到诊断的全面赋能双特异性抗体的独特机制使其在多个医学领域实现价值落地,从疾病治疗到诊断成像,形成了多元化的应用场景:在癌症治疗领域,双抗是研发最为集中的方向,尤其在血液肿瘤(白血病、淋巴瘤、多发性骨髓瘤)中进展迅速 —— 这类肿瘤细胞呈悬浮状态,易于与抗体接触,双抗的 “精准桥接” 优势得以充分发挥,多款药物已进入临床应用或后期研发阶段。相比之下,实体瘤治疗面临肿瘤微环境屏障、靶点异质性等挑战,仍是双抗研发的重点突破方向,目前研究多聚焦于优化抗体穿透性、靶向肿瘤微环境关键靶点等策略。
在自身免疫性疾病领域,双抗的设计核心是同时中和两种致病性细胞因子,例如靶向 TNF 与 IL-17A 的双抗,可同时阻断两条关键炎症通路,相较于两种单抗联用,不仅能提升疗效,还能通过协同作用减少单个细胞因子过度抑制带来的副作用,在类风湿关节炎、银屑病等疾病中展现出良好的应用前景。
在临床诊断领域,双抗凭借 “双抗原结合” 的特异性优势,成为高灵敏度检测技术的核心元件:其一端可特异性结合病原体抗原(如结核杆菌 LAM 抗原、乙肝表面抗原),另一端结合辣根过氧化物酶(HRPO)等信号酶,通过信号放大效应,可开发快速检测试纸条或 ELISA 试剂盒,实现对病原体的精准、快速筛查,大幅提升诊断效率。
在医学影像领域,双抗采用 “预靶向” 创新策略,解决了传统影像试剂信噪比低、肿瘤定位不精准的问题:先向患者注射能同时识别肿瘤抗原(如 CEA)和小分子肽(如 HSG)的双抗(如 TF2),待抗体在肿瘤部位富集且血液中多余抗体被清除后,再注射放射性标记(如 68Ga)的小分子肽(IMP288),该肽会与肿瘤部位的双抗特异性结合,实现高信噪比的肿瘤免疫 PET 成像,尤其擅长检测直径小于 1cm 的微小肿瘤,为肿瘤早期诊断与疗效评估提供了全新工具。
三、总结与展望双特异性抗体通过工程化改造实现了 “一药双靶” 的精准调控,其核心优势在于兼顾靶向特异性与功能多样性,既突破了传统单抗的治疗局限,又拓展了抗体技术在诊断、影像等领域的应用边界。从肿瘤治疗的 “免疫桥接” 到自身免疫病的 “炎症双阻”,从临床诊断的 “精准检测” 到医学影像的 “微小病灶识别”,双抗正以多场景赋能的姿态,推动生物医学向 “精准化、高效化” 升级。
目前,双抗研发仍面临部分挑战:实体瘤的微环境穿透、抗体生产工艺的稳定性、长期安全性评估等问题,仍需通过蛋白质工程优化、给药策略创新等方式逐步解决。未来,随着合成生物学、AI 辅助抗体设计等技术的融合应用,双抗将朝着 “多靶点协同、低毒性、高稳定性” 方向发展,不仅将在更多疾病领域实现临床转化,还可能与细胞治疗、基因治疗等技术联合,构建更高效的疾病干预体系,成为生物医学领域的核心支撑技术之一。
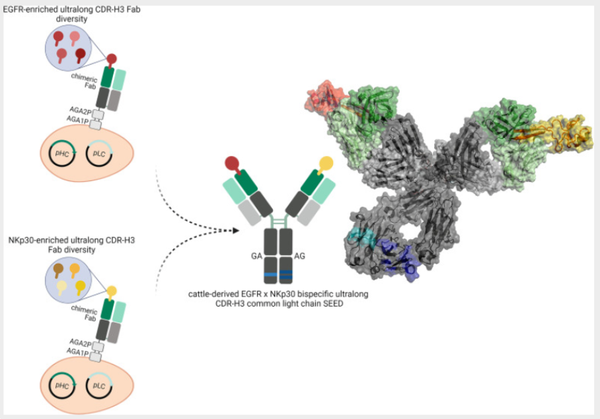
图源:https://zhuanlan.zhihu.com/p/579402653