1月20日,CDE官网显示,百利天恒1类新药注射用BL-B01D1新适应症上市申请获受理,用于既往经PD-1/PD-L1单抗联合含铂化疗治疗失败的复发性或转移性食管鳞癌患者。此前,该适应症已被CDE纳入优先审评。
BL-B01D1(Iza-bren,伦康依隆妥单抗)是一款全球首创双抗ADC,通过双重作用机制阻断EGFR和HER3向肿瘤细胞传递的信号,从而抑制其增殖与存活信号。此外,通过抗体介导的内吞作用,BL-B01D1释放的治疗性有效载荷可引发基因毒性应激,最终导致肿瘤细胞死亡。
2023年12月,百利天恒与BMS达成合作,BL-B01D1在中国由百利天恒独家开发,在中国以外的地区由西雅图免疫与百时美施贵宝共同开发,总金额高达84亿美元,其中首付款8亿美元。
2025年9月,BL-B01D1的首个鼻咽癌适应症被CDE纳入优先审评。2025年11月,BL-B01D1的鼻咽癌适应症的新药上市申请被CDE正式受理。Insight数据库预测该适应症有望在今年下半年获得批准。
2025年11月,BL-B01D1治疗食管鳞癌的III期研究(研究方案编号:BL-B01D1-305)在预设的期中分析中达到了无进展生存期(PFS)和总生存期(OS)显著延长的双重主要终点。这也是全球首个ADC药物在食管癌治疗中取得PFS和OS双阳性结果的III期临床研究。
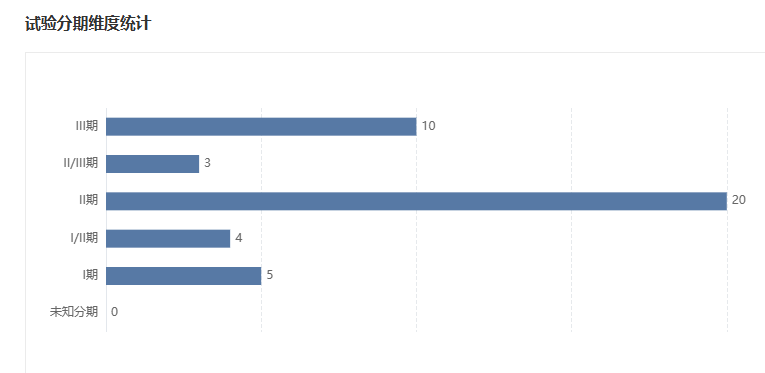
目前,BL-B01D1正在中国和美国进行40余项针对多种肿瘤类型的临床研究,其中包括在NSCLC、SCLC、鼻咽癌、乳腺癌、尿路上皮癌、食管癌等多种实体瘤中开展的10项III期临床研究。
Insight数据库显示,目前全球范围仅有10款生物药新药用于食管癌治疗,1款为伊匹木单抗(CTLA4单抗)、1款为尼妥珠单抗(EGFR单抗),以及8款PD-(L)1单抗,包括信迪利单抗、替雷利珠单抗、卡瑞利珠单抗、帕博利珠单抗、纳武利尤单抗等,但尚未有ADC获批。如果本次适应症获得批准,BL-B01D1将成为全球首个适用于食管癌治疗的ADC药物。
文章内容仅供参考,不构成投资建议。投资者据此操作,风险自担,关于对文中陈述、观点判断保持中立,不对所包含内容的准确性、可靠性或完整性提供任何明示或暗示的保证。请读者仅作参考,并请自行承担全部。