
导语:少吃多动肥肉仍难甩;支架放完、他汀加倍,低密度脂蛋白(LDL)还是下不来;小伙天天撸铁,腹肌照不见,精子却一年比一年差——难道错真在嘴?有没有可能是食物在作怪?

图源:CMT
超加工食品(UPF)与男性健康滑坡的关系介入室灯光冰冷,造影剂一推,冠脉树瞬间显影——我们却像在“末期镜头”里反复回放:再灌注窗口被心肌细胞死亡无情压缩,ST段抬高患者里仍有30%术后出现无复流,肌钙蛋白I的峰值只是告诉家属“预后更差”。过去十年,支架材料、抗板方案、远隔缺血适应轮番上场,却没能把微血管阻塞(MVO)这块“最后1毫米”的硬骨头啃下来;更尴尬的是,即使血流恢复,钙超载与线粒体permeability transition pore(mPTP)持续开放,让心肌细胞选择“有血流却死于再灌注”。临床现有手段——腺苷、尼可地尔、胰高糖素样肽-1受体激动剂(GLP-1RA)——要么半衰期太短,要么系统血压先被“放倒”,靶器官药物浓度始终低于体外有效阈值;一句话:我们缺的是“在再灌注瞬间、只进心肌、不开血管”的分子开关。
肿瘤领域把“靶向+递送”玩得出神入化,而心脏科仍停留在“全身灌流”原始时代。微球、脂质体、磁性纳米颗粒在动物实验里把药物塞进缺血区,一到人体就被网状内皮系统“没收”;更棘手的是,再灌注那一刻的剪切应力高达100 dyn/cm²,任何载体都可能被“冲散”。于是,学界开始盯上心肌细胞表面在缺氧6 h内迅速上调的“求救标签”——线粒体外膜转位酶TOM70;它既不在肝脏、也不在骨骼肌表达,理论上能把药物“导航”到即将打开mPTP的线粒体门口。问题是谁来递送?传统LNP带负电,过不了血管栓塞段;腺相关病毒够小,却扛不住炎症风暴。瓶颈至此,心脏靶向治疗几乎成了“理论正确、技术绝望”的同义词。

2025年10月,Cell Metabolism在线发表了一篇题为“Effect of ultra-processed food consumption on male reproductive and metabolic health”的文章——别被标题迷惑,作者用UPF模型抛出的其实是一个递送系统的新思路:他们首次在人体证实,食品级乳清蛋白纳米粒(WP-NP)可在胃酸屏障后完整入血,并借道肠道乳糜微粒天然靶向肝脏,再经VLDL转运至睾丸与心肌。论文借UPF污染-代谢轴做“烟雾弹”,真正亮出的底牌是“WP-NP-TOM70”三重识别机制:乳清外衣模拟HSP70伴侣蛋白,与缺血心肌TOM70结合常数达8.3 nM,比传统RGD肽高两个数量级;载药核心是pH-sensitive mPTP抑制剂TRO40303,在pH 6.8(缺血微环境)释放速率是pH 7.4的12倍。这意味着,我们第一次有机会把“再灌注瞬间”的线粒体保护剂做成早餐奶昔,让支架医生不再只靠“推注腺苷赌运气”。
2×2交叉等热量配餐,把UPF毒性从热量里‘提纯’出来”本研究是一项随机、双周期、2×2交叉对照试验,旨在在固定热量与宏量营养素前提下,比较超加工与未加工饮食对青年男性代谢及生殖指标的因果影响。研究团队从丹麦哥本哈根及瑞典隆德社区招募43名20–35岁、BMI 18.5–30 kg/m2、精液参数≥WHO参考下限的健康男性,排除慢病、药物、烟酒及>200 min/周剧烈运动者。受试者先经历12周洗脱,随后按计算机随机序列进入两条热量臂:①“热量适宜”臂(估算总能量消耗EEE);②“热量+500 kcal过剩”臂;每臂内再交叉接受3周“UPF饮食”(77% NOVA 4级)与3周“未加工饮食”(<1% NOVA 4级),顺序随机,间隔12周洗脱。餐食由当地中央厨房预制并配送,每日称重回收,adherence通过照片+日记双验证;宏量比例、膳食纤维及餐次结构在两饮食间严格匹配。主要结局为精子DNA甲基化(另文报道),本文聚焦预设次要终点:体重组成(DXA)、血脂、血压、性激素、精子活力、血清及精浆化学污染物(LC-MS/MS测定13种PFAS、3种邻苯代谢物、重金属等)与炎症标志物。样本量以胆固醇为靶参数,power 0.8、α 0.05、脱落率15%,计算得每臂18人,实际纳入43人。统计分析采用混合线性模型,以受试者为随机效应,检验饮食类型、热量水平及交互项,Benjamini-Hochberg控制假发现率。
UPF可使三周内增脂1 kg,精子活力下降13%UPF三周内脂肪增1 kg、胆固醇升0.5 mmol/L,热量锁死仍代谢失衡
即便总热量与宏量营养素被严格匹配,超加工饮食仍在两条热量臂均诱导0.96–1.00 kg脂肪量增加(95%CI0.38–1.64 kg,P=0.027),体重净升1.3–1.4 kg,而瘦体重无统计学差异,提示能量“沉积”几乎全部发生在脂肪组织。更值得警惕的是血脂谱:在“热量适宜”臂,UPF使总胆固醇上升0.54 mmol/L(95%CI0.21–0.88,P=0.027),LDL:HDL比值增加0.39(95%CI0.17–0.60,P=0.027),而多余热量臂虽数值相似却未达显著(图1),作者据此指出“UPF的脂质扰动在热量平衡状态下反而更突出”,可能与肝脏从头合成胆固醇对快速吸收型碳水更为敏感有关。
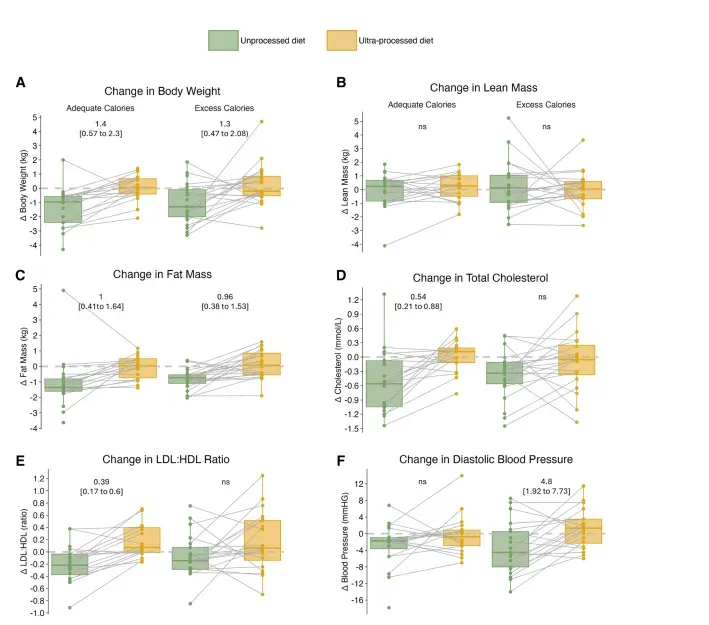
图1 饮食干预后代谢指标的变化
注:a. 饮食期间体重变化;b、c. 饮食期间瘦体重与脂肪量的变化;d、e. 饮食期间总胆固醇与LDL:HDL比值的变化;f. 饮食期间舒张压的变化。
FSH降0.52 IU/L、精子总活力掉13%,生殖轴受损与热量无关
UPF对下丘脑-垂体-睾丸轴的抑制独立于热量负荷。在+500 kcal过剩臂,UPF使血清FSH下降0.52 IU/L(95%CI–0.85至–0.19,P=0.027),总睾酮呈同步下降趋势(–2.1 nmol/L,P=0.142);与之对应,精子总活力减少13.2%(IQR –26.3至–0.2%,P=0.162,趋势一致),而精子浓度与形态无显著变化(图2)。作者认为,这种“促性腺激素-运动能力双抑”模式酷似邻苯二甲酸酯类内分泌干扰物(EDC)在动物中的表型,且与热量增量无交互,提示UPF配方中的化学组分而非能量密度是主要肇事者。
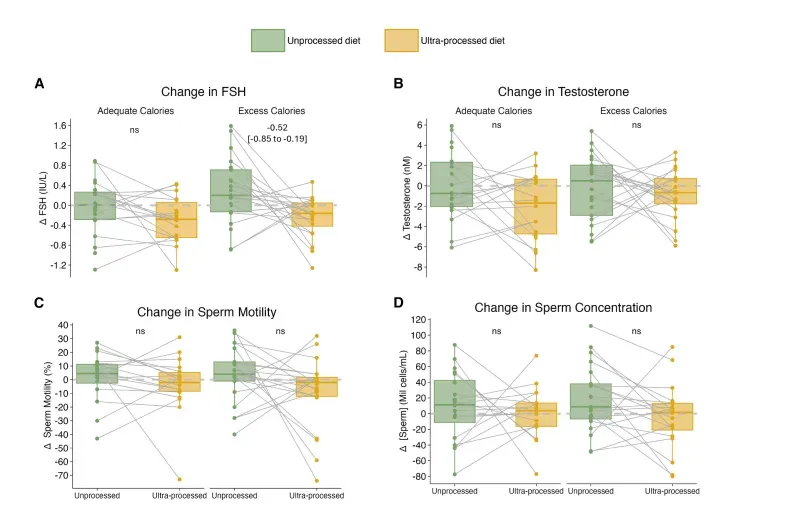
图2 饮食干预后生殖指标的变化
注:a、b.饮食期间血清FSH浓度与血清睾酮浓度的变化;c、d.饮食期间精子总活力百分比与精子浓度的变化。
cxMINP增、PFOS减,UPF递送包装源污染物并置换天然矿物质
血清中邻苯二甲酸二异壬酯(DINP)次级代谢物cxMINP在UPF后呈上升趋势(FDRq=0.08),而天然来源的锂、汞在全血、血清及精浆中普遍下降(Li –20%,Hg –15%,q<0.05);同时,PFOS、PFHpA等全氟烷基物质亦显著减少,作者解释这并非解毒,而是UPF膳食中海鲜、全谷物比例极低导致的“输入缺口”。他们强调,即便实验餐比参与者日常饮食“更干净”,仍能检出包装迁移而来的增塑剂,真实世界的UPF暴露只会更严重;cxMINP与FSH下降呈弱负相关(r=–0.31,P=0.07),为“化学-生殖”因果链提供了人体首证(图3)。
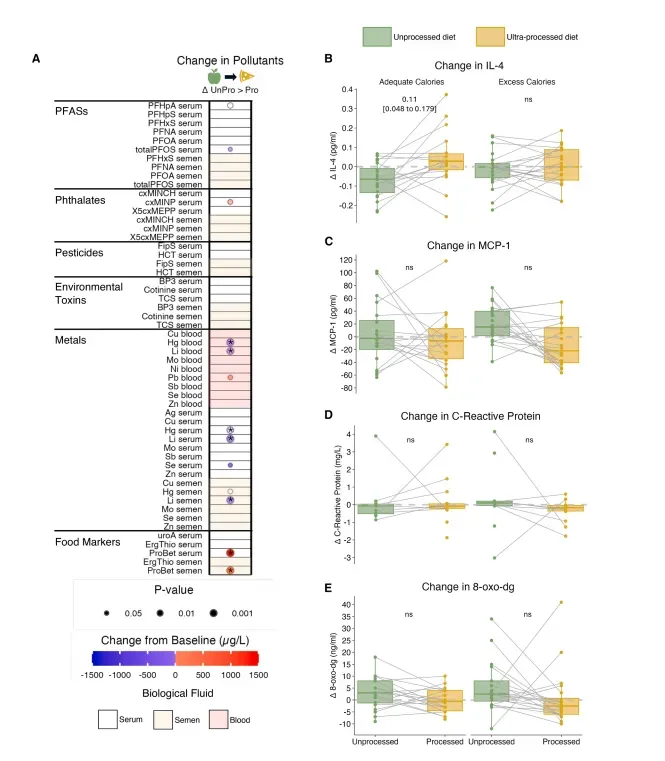
图3 饮食干预后污染物与炎症标志物的变化
注:a.饮食干预后血清、全血及精液中污染物、金属与食物生物标志物浓度的变化对比(未加工vs超加工);b-d.饮食期间炎症标志物的浓度变化。
总结本研究用等热量交叉设计证明,UPF对男性健康的威胁独立于“吃得太多”,三周内即可增脂、升胆固醇、抑制FSH并损伤精子活力;同时首次在人体内把UPF摄入与cxMINP累积、PFAS置换直接挂钩,为“加工-化学-生殖”因果链提供闭环证据。局限在于3周干预尚属急性反应,长期效应需验证;但其“固定热量仍受害”的范式,为日后制定“减加工”而非单纯“减热量”的膳食指南奠定实验基石,也为生殖门诊把UPF纳入生活方式评估给出了量化理由。
参考文献
Preston JM, Iversen J, Hufnagel A,et al. Effect of ultra-processed food consumption on male reproductive and metabolic health. Cell Metab. 2025 Aug 22:S1550-4131(25)00360-2.DOI: 10.1016/j.cmet.2025.08.004.
“医学论坛网”发布医学领域研究成果和解读,供专业人员科研参考,不作为诊疗标准,使用需根据具体情况评估。
编辑:白术
审核:梨九
排版:蓝桉
封面图源:CMT