基因病患者的家属最懂这种痛:眼睁睁看着亲人被遗传缺陷折磨却无能为力。
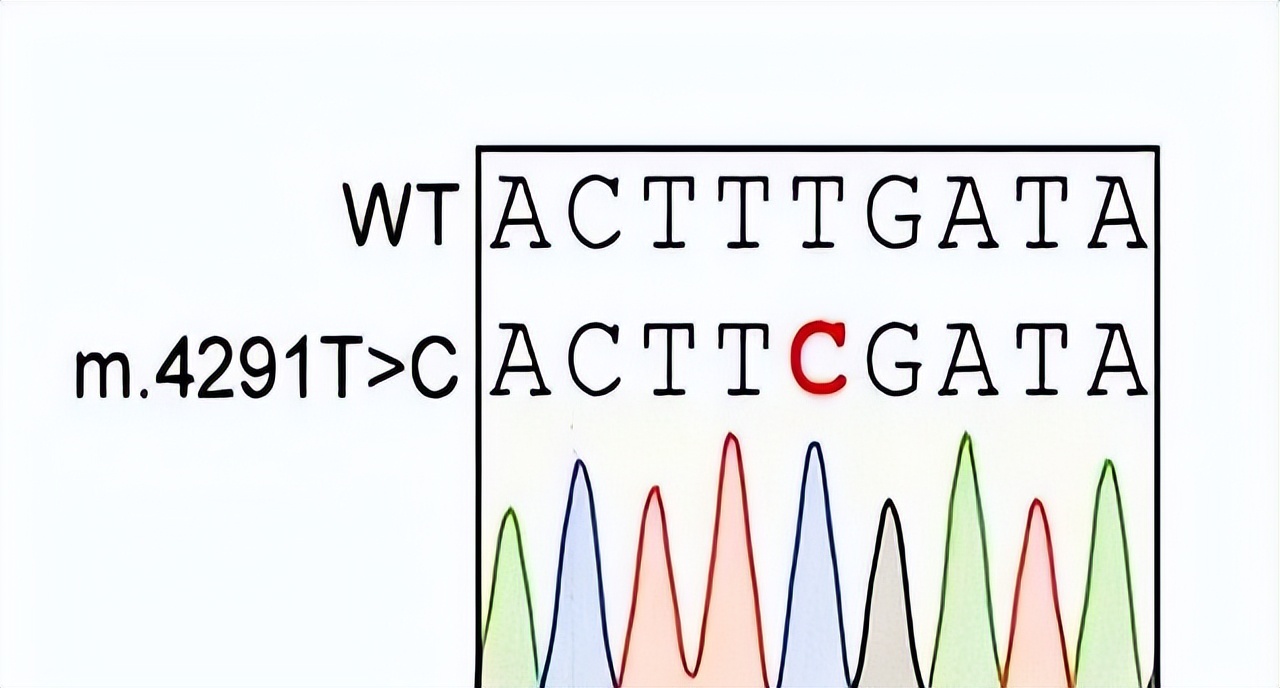
特别当医生说出"线粒体DNA异常"时,很多家庭瞬间被绝望笼罩——这些遗传密码错误能引发200多种重疾,且传统基因编辑工具根本够不着线粒体里的基因。直到荷兰科研团队在《PLOS Biology》扔出震撼弹:用DdCBE技术成功修改线粒体DNA,把患者细胞里的错误遗传密码精准修正,连线粒体膜电位都恢复了。

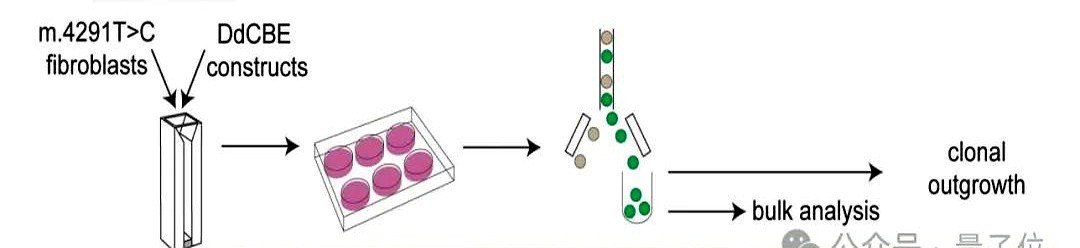
这次突破的妙处在于绕过CRISPR玩不转的困局。搞过基因编辑的都懂,CRISPR这把"基因剪刀"虽然牛,但根本进不了线粒体这间密室。荷兰科学家直接换赛道,搞出DdCBE这个不依赖CRISPR的编辑器。它就像会开锁的纳米机器人,带着编程好的TALE蛋白定位系统,精准找到线粒体里的特定碱基进行替换,连DNA链都不用切断。他们在患者类器官里成功构建致病突变,又在患者成纤维细胞中修正变异,实测线粒体功能确实改善——虽然ATP产量提升不明显,但这至少证明治疗窗口存在。
不过真要在临床落地,还有几座大山要翻。看看实验数据就知道,编辑效率在细胞之间波动大到离谱,有的细胞能修正81%,有的压根没动静。更诡异的是在能量代谢测试时,线粒体功能恢复的稳定性像抽盲盒,同一批处理细胞结果天差地别。这说明目前技术对细胞个体差异的掌控力还不足,搞不好会治出个"细胞社会"——部分细胞痊愈,部分纹丝不动。这要放在人体里,可能造成不可预测的连锁反应。

递送系统倒是让人眼前一亮。用脂质纳米颗粒包裹modRNA递送编辑器,这招既避开病毒载体的安全风险,又实现96%以上的转染率。但问题来了,编辑过的线粒体DNA到底能不能长期稳定?在培养皿里观察50天可能不够,毕竟线粒体DNA复制机制和核DNA不同,说不准哪天突变的DNA又反攻倒算。更别说核基因组里发现的微量脱靶编辑,虽然目前检测不到显著危害,可谁敢保证这些随机突变不会埋雷?
回看人类攻克基因病的历程,从1990年首例基因治疗到CRISPR获批临床,每次突破都要经历十几年验证。这次线粒体编辑虽然曙光初现,但参考眼下手游治病案例的进展速度,估计三五年内能进一期临床就算神速。不过对挣扎在生死线的患者来说,至少看到了改写命运的可能——毕竟这是人类首次在细胞层面修复线粒体这个"能量工厂"的底层代码。